Biologie stárnutí a stresu
Řada přírodních látek má prokazatelné účinky na některé biochemické a buněčné parametry se vztahem ke stresu, stárnutí a nemocem souvisejícím se stárnutím a stářím. Účinky kandidátních látek (včetně např. fytohormonů) jsou studovány na primárních lidských liniích a na modelovém organismu Caenorhabditis elegans. Očekávané indikace zahrnují poruchy spánku, neurodegenerativní onemocnění a stárnutí kůže. V oblasti dermatologie a kosmetiky je cílem identifikace látek pro terapii poruch pigmentace (hodnocení melanogeneze) a psoriázy (diferenciace keratinocytů). Vyvíjíme také látky s vylepšenou schopností dosáhnout hlubokých vrstev kůže. Hlístice Caenorhabditis elegans je také využívána jako model pro vyhledávání nových antihelmintik. Studujeme také mechanismy rezistence želvušek (Tardigrada) k radiaci. Testované látky a molekulární cíle jsou vyhledávány pomocí bio- a cheminformatických metod.
Členové týmu: Jiří Voller, Alena Kadlecová, Václav Mik, Dominika Trofimenková, Tomáš Jirsa

Farmakognosie a metabolomika
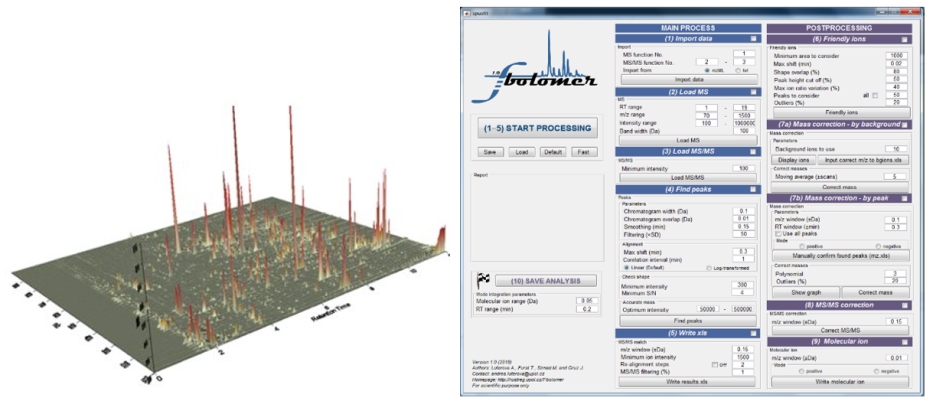
Výzkum skupiny je zaměřen na vyhledávání nových biologicky účinných metabolitů a biomarkerů v rostlinách, houbách, bakteriích a dalších organismech. Přírodní produkty představují bohatý zdroj látek s potenciální biologickou aktivitou a i dnes jsou inspirací pro vývoj nové generace léčiv. Zaměřujeme se proto na jejich izolaci, charakterizaci a ověřování účinku v různých biologických systémech. Účinné sloučeniny mohou sloužit nejen jako samotné bioaktivní molekuly, ale také jako předlohy pro syntézu derivátů s vylepšenými vlastnostmi a vyšší selektivitou.
Účinné látky jsou identifikovány pomocí moderních metabolomických a bioinformatických metod, přičemž vývoj těchto metod je rovněž jedním z hlavních cílů naší práce. Zvláštní důraz klademe na vývoj výpočetních nástrojů a softwaru pro zpracování LC-QTOF-MS dat, který umožňuje efektivní identifikaci aktivních metabolitů. Tyto přístupy rozšiřují možnosti korelační metabolomiky a poskytují hlubší porozumění vztahu mezi chemickou strukturou přírodních látek a jejich biologickými účinky.
Ve spolupráci s dalšími výzkumnými skupinami vyhledáváme sloučeniny s protizánětlivými, antioxidačními, antiproliferačními, antimikrobiálními či anthelmintickými vlastnostmi. Obecně se soustředíme na látky, které mohou zasahovat do klíčových buněčných procesů, jako je proliferace, apoptóza, angiogeneze nebo obranné mechanismy rostlin. Tyto biologické aktivity jsou zásadní nejen pro pochopení fungování živých systémů, ale také pro nalezení nových možností v léčbě závažných onemocnění, včetně rakoviny či chronických zánětlivých chorob.
Speciální pozornost je věnována vlivu nízkomolekulárních metabolitů na růst, vývoj a reprodukci rostlin. Tyto procesy jsou modelovým systémem, který nám umožňuje sledovat, jak malé bioaktivní molekuly ovlivňují složité biologické dráhy. Zároveň tyto poznatky otevírají prostor pro využití v zemědělství a biotechnologiích, kde mohou nové látky přispět k ochraně rostlin, zvýšení jejich odolnosti nebo optimalizaci růstu.
Členové týmu: Jiří Grúz, Klára Končáková, Andrea Kosinová, Amálie Mikulková
Inhibitory proteinkinas
Fosforylace představuje univerzální mechanismus regulace struktury, lokalizace, aktivity a stability proteinů zapojených prakticky ve všech buněčných procesech. Odhaduje se, že 10-50 % proteinů může být fosforylováno, často i na mnoha místech najednou. Fosforylaci katalyzují enzymy ze skupiny proteinkinas a jejich změny mohou být příčinou řady onemocnění a poruch. Četné abnormality vztahující se k aktivitám proteinkinas byly idenfikovány také v nádorech. Geny kódující proteinkinasy bývají mutovány, amplifikovány a translokovány, což v důsledku výrazně mění chování buněk a podstatnou měrou přispívá k jejich nádorové transformaci. Pochopení těchto molekulárních změn iniciovalo vývoj nízkomolekulárních inhibitorů proteinkinas, které zasahují důležité buněčné procesy a uplatňují se nejen jako nástroje v buněčné biologii, ale zejména jako léčiva pro nádorová onemocnění.
Vývoj inhibitorů proteinkinas jako potenciálních protinádorových léčiv probíhá také v naší laboratoři. Systematicky navrhujeme, připravujeme a studujeme sloučeniny na bázi purinu a jemu isosterních heterocyklických systémů, jako jsou například 8-azapuriny, pyrazolo[4,3-d]pyrimidiny, pyrazolo[4,3-e][1,2,4]triaziny, imidazo[4,5-c]pyridiny nebo imidazo[1,2-c]pyrimidiny. Některé naše inhibitory vykazují nanomolární aktivitu v buněčných i v myších modelech rakoviny. Zabýváme se nejen osvědčenými kompetitivními inhibitory, ale také moderními modulátory stability kinas na bázi cílené degradace technologií PROTAC. Mezi studované enzymy patří zejména cyklin-dependentní kinasy (CDK) a receptorové kinasy FLT3 a PDGFR.
Některé nízkomolekulární inhibitory proteinkinas se dnes již běžně používají jako léčiva, nicméně řada onkologických onemocnění zůstává stále odkázána na klasická cytostatika, jejichž používání provází nepříjemné vedlejší účinky. Proto považujeme tuto oblast výzkumu za velmi atraktivní a vývoj inhibitorů proteinkinas na méně probádaných heterocyklických systémech je jedním z našich současných výzkumných záměrů.
Členové týmu: Vladimír Kryštof, Eva Řezníčková, Radek Jorda, Tomáš Gucký, Václav Mik, Miroslav Peřina, Veronika Vojáčková, Petra Krňávková
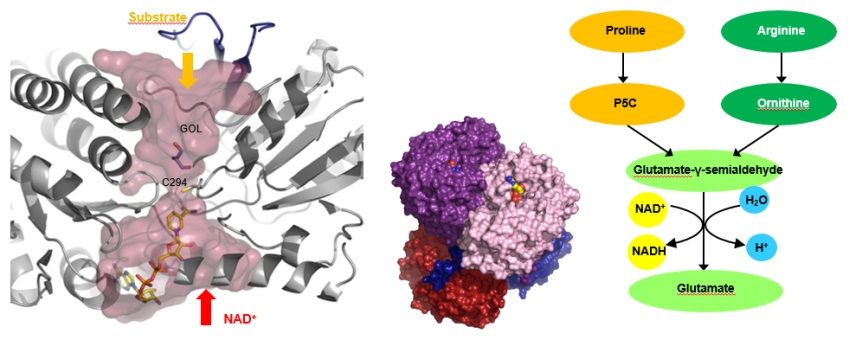
Strukturní biologie
Skupina se dlouhodobě zabývá studiem funkce proteinů in vitro a in vivo, jejich strukturou a vazebnými interakcemi s ligandy (metabolity). Výzkum je zaměřen na dva hlavní tematické okruhy:
Prvním okruhem je nadrodina rostlinných a lidských aldehyddehydrogenas (ALDHs), které oxidují biogenní a xenobiotické aldehydy pomocí NAD(P)+. Aldehydy jsou velmi reaktivní sloučeniny a jsou generovány během metabolismu sacharidů, vitamínů, biogenních aminů, aminokyselin, steroidů a lipidů. ALDH jsou obecně považovány za detoxifikační enzymy tím, že se účastní adaptivní odpovědi na abiotický stres a aldehydy eliminují. V průběhu posledních deseti let jsme charakterizovali rostlinné rodiny ALDH2 (PDB ID: 4PXL, 4PZ2), ALDH7 (PDB ID: 4PXN), ALDH10 (PDB ID: 3IWK, 3IWJ, 4I8P, 4I9B, 4IQ8), ALDH12 (PDB ID: 6D97), a ALDH21 (PDB ID: 5MZ5, 5N5S, 5MZ8) a lidské ALDH7 a ALDH9 (PDB ID: 6QAK, 6QAO, 6QAP).
Druhým okruhem jsou enzymy a proteiny účastnící se metabolismu a percepce rostlinných hormonů cytokininů, které regulují základní rostlinné procesy včetně buněčného dělení, vývoj meristémů, stonku, kořene, semen a senescenci. Jde o rodiny cytokininoxidas/dehydrogenas (CKO/CKX, PDB ID: 4O95, 3S1C, 3S1D, 3S1E, 3S1F, 4MLA, 4ML8, 4OAL, 3KJM, 2QKN, 2QPM, 5HQX, 5HMR, 6YAO, 6YAQ, 6YAP), nukleosid-N-ribohydrolas (NRH, PDB ID: 4KPN, 4KPO), adenosinkinas (ADK), adeninfosforibosyltransferas (APRT) a histidinkinasových receptorů obsahujících CHASE doménu. Modulace hladin cytokininů, skrze tyto enzymy, představuje možnost zlepšení některých vlastností zemědělských plodin (např. výnos nebo odolnost vůči abiotickému stresu) v budoucnu.
Výzkum zahrnuje techniky heterologní exprese genu kódujícího studovaný protein v E. coli, kvasinkách nebo Arabidopsis thaliana, přípravu overexpressorových či knockout linií v mechu Physcomitrella patens ve spolupráci s pracovištěm na Univerzitě v Hamburku (Dr. Klaus von Schwartzenberg) či RTG krystalografie ve spolupráci s pracovišti na IJPB INRA Versailles (Dr. Pierre Briozzo) a na I2BC Univerzitě Paris-Saclay (Dr. Solange Moréra). U enzymů jsou analyzovány kinetické parametry substrátů a inhibitorů; vazebné parametry mezi proteinem a ligandem jsou studovány pomocí termoforézy v malém měřítku (MST). Další techniky představují metody qPCR, za účelem sledování změn v expresi genů, místně-řízenou mutagenezi spojenou se studiem vazebného/aktivního místa proteinů, nanodiferenciální skenovací fluorometrii (nanoDSF) spojenou se studiem stability proteinů, a CD spektrometrii, jež slouží ke studiu sekundárních struktur.
Členové týmu: David Kopečný, Martina Kopečná, Radka Končitíková, David J. Kopečný, Jakub Bělíček